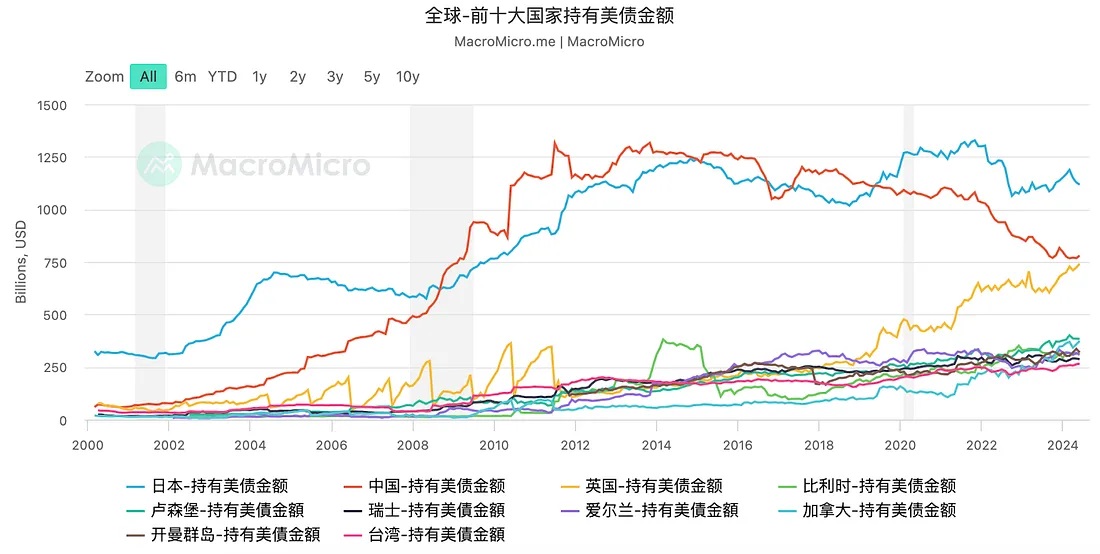
近期,由日元套息交易退潮带来的一场剧烈市场波动让人们把目光投向日本央行的货币政策,叠加美联储降息预期的不确定性,市场一片风声鹤唳。本文通过一些历史事件梳理和经济学的基本原理为大家简要梳理日元避险货币属性的由来。历史上日本总有办法利用自身独特的货币政策和套息交易重新调节日元汇率,而这次是否不一样?
最后,本文想借日元汇率和价值的影响因素分析,引出对国家储备资产的思考。接下来的文章也将继续从经济学理论的角度去探讨货币的价值和比特币的信仰这一话题,因此,本篇也可以看做一篇引文。
正文
1. 日本常年维持低利率的历史背景
近期,由日元套息交易退潮带来的一场剧烈市场波动让人们把目光投向日本央行的货币政策,叠加美联储降息预期的不确定性,市场一片风声鹤唳。
日元的套息交易历史由来已久。而日元超低利率的历史还要追溯到上个世纪80年代,美国对日本发动贸易战。
在20世纪80年代,受到70年代布雷顿森林体系解体和石油危机的影响,美国经历了历史上最严重的“大通胀”,时任美联储主席保罗沃尔克采取了暴力加息的方式以抑制通胀,导致美元在国际市场上迅速升值。虽然这在一定程度上吸引了国际资本流入美国,但也造成了美国出口商品在国际市场上变得更加昂贵,进一步加剧了美国的贸易赤字。
在1970年代至1990年代,美国对当时的世界第二强国、当时美国最大的贸易伙伴日本发起了漫长的贸易战和汇率战。
日美贸易战前后围绕纺织品、钢铁业、彩电业、汽车产业、半导体产业进行,伴随着日本的产业结构转型和新兴科技的发展。长达30年的贸易战并未如美国所预期的那样阻止日本相关产业的发展,也没有解决美国贸易不平衡的问题。
但汇率战的结果相当显著。20世纪80年代初期,美元兑日元一直处于250左右的高位。1985年9月22日由美国、日本、西德(现德国)、法国和英国的财政部长和中央银行行长在纽约广场饭店(Plaza Hotel)签署了《广场协议》。该协议的主要目的是通过协调干预外汇市场来削弱美元的汇率,从而缓解美国的贸易赤字,特别是对日本和西德的巨额贸易赤字。
协议达成后,各国同意采取联合干预的措施来压低美元汇率。结果,日元相对于美元迅速升值。此后,尽管日本下调了政策利率,但日元仍继续升值。
由于当时日本GDP主要来源于出口,为了减少日元升值对出口的负面影响,日本央行被迫长期维持低利率,帮助企业获得资金支持,促进社会投资和经济增长。这一政策也直接促成了日本房地产泡沫。
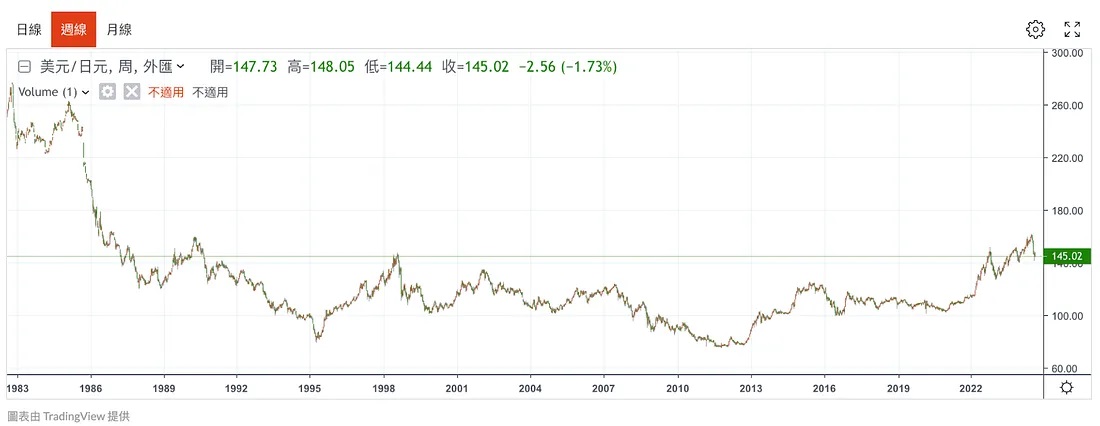
图:美元/日元汇率历史走势
即使当前美国对日本的贸易战早已结束,但是久而久之形成的日本长期货币政策体系和地产泡沫破裂后的资产负债表衰退对日本造成的经济伤害仍在。
回顾近年来日本央行为维持日元价值稳定所做的一些货币政策操作如下:
2008 年金融危机以后,日本央行为振兴经济将利率降为0%,并施行货币宽松政策(QE),大规模购买资产;
2013年安倍上台后,实施质化与量化宽松政策(QQE),将政策目标定为控制基础货币、增加购买政府国债、日股等资产,以及延长政府国债到期上限、提高预期通胀、降低实际利率、促使日元贬值带动出口;
2016年1月,在安倍经济学效果减缓的情况下,日本央行改实施负利率政策;
2016年9月,日本央行维持负利率决议与资产购债规模,但放弃货币基础为目标,改推出控制收益率曲线YCC,将10年期国债收益率维持在 0%,以保障金融业获利空间。
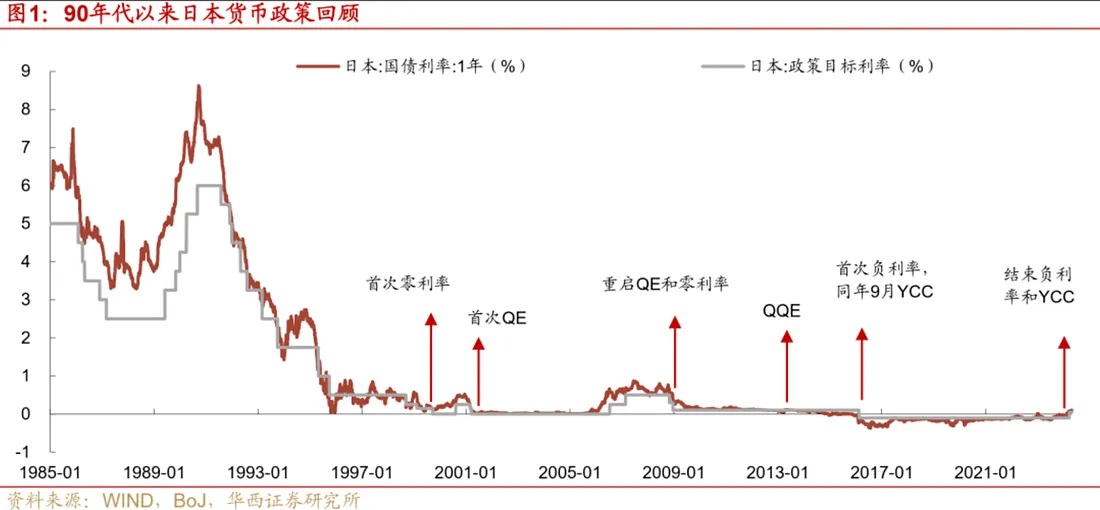
这些政策保证了日元长期处于低利率区间,尽管低利率最终引发了房地产泡沫破裂,导致日本长期处于通货紧缩状态,但也因此使得日元成为国际套息交易的主要融资货币。
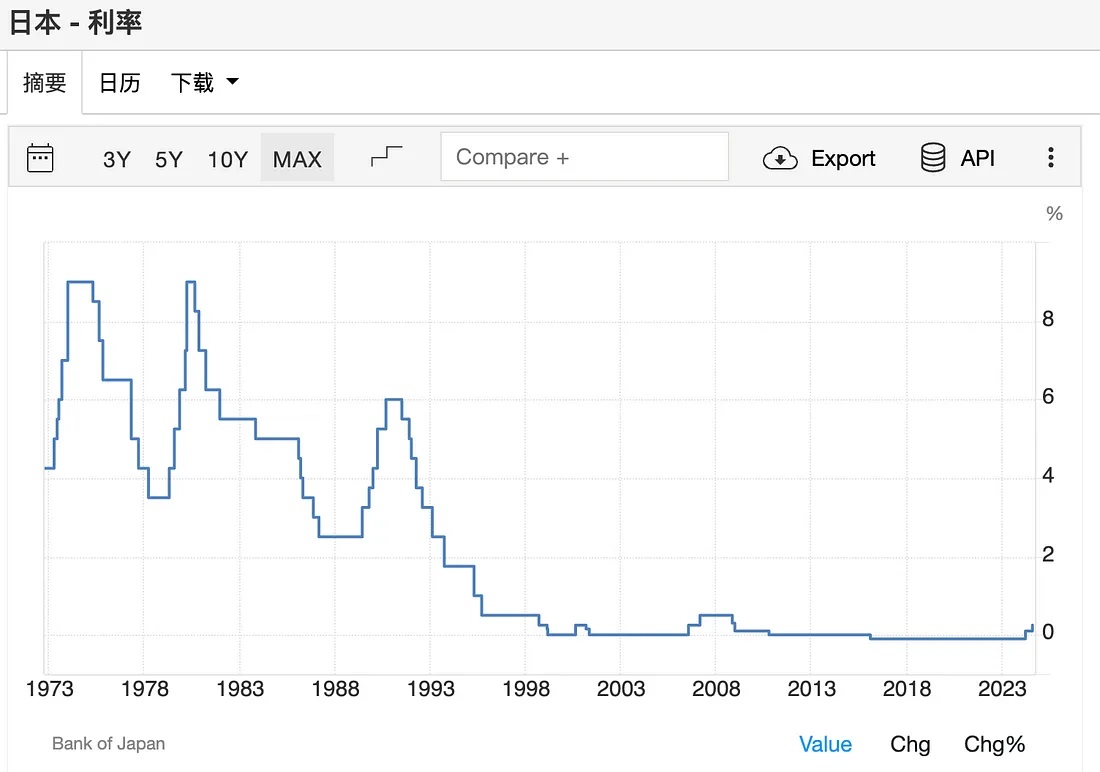
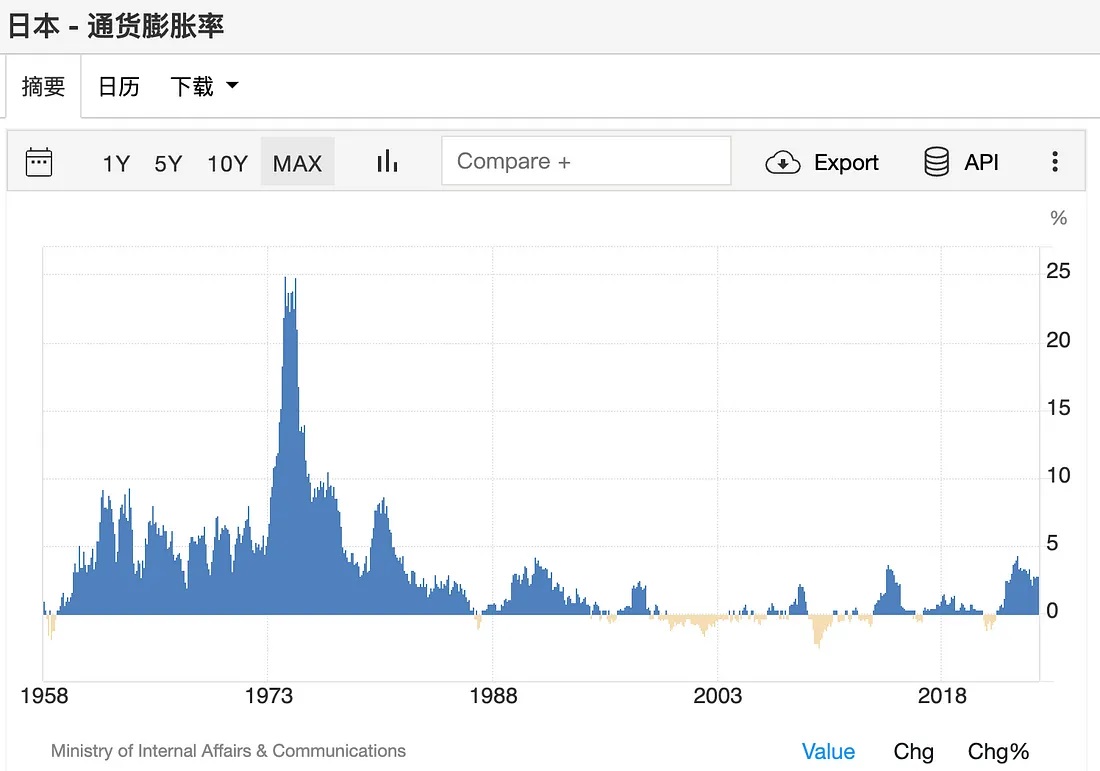
2. 套息交易的发展催生日元的避险属性
所谓的套息交易(Carry Trade)是国际外汇市场常见的一种交易行为,在套息交易中,外汇投资者借入低息货币(如日元),并将买入的高息货币投资于其国内的无风险资产(国债为主),从而赚取两种货币所对应的无风险资产的息差,其本质上是一种外汇投机行为。而息差的存在是进行套息交易的主要驱动因素。
对于套息交易来说,这是一种跨境资产配置的投资方式,需要比较国内资产与国外资产的预期回报率。在考虑将货币资产投资到更高收益的金融产品中之前,首先应考虑投资外币的预期回报率。
以美日套息交易为例,套利者借出日元去投资美元资产时,预期回报率应当考虑美元的升值或贬值预期,因为未来计算投资回报时需要转换回融资货币(日元)(根据利息平价条件,只有当汇率使得国内资产和国外资产的预期回报率相等时,投资者才愿意持有国内资产)。因此,以日元衡量美元资产的预期回报率,等于美元资产利率与美元预期升值率/贬值率之和。
因此,日元套息交易在美元加息之前其实主要是利率相对更高的澳元而非美元,近年来美元加息带来的利差扩大和升值预期才使其成为更重要的投资标的。
套息交易作为一种外汇投机行为,汇率的变化自然是重要考虑因素。经济学世界里,汇率的影响因素主要有通货膨胀、利率和国际收支平衡。参照美日贸易战和汇率战,在政治上,国际贸易保护主义也是十分重要的影响因素。
从经济学角度来看,前两个因素可以用购买力平价理论和利率平价理论来理解。
购买力平价理论(Purchasing Power Parity, PPP)是国际经济学中的一个基本理论,在相对长的周期内可以对汇率的表现进行解释。一种绝对的购买力平价理论认为:如果没有运输成本、关税以及其他贸易障碍,同一种商品在不同国家的价格应该是相同的,如果同样一件商品的价格只能用一种货币表示时(比如都用美元计价),那么作为商品生产国的货币(比如日元)与这一计价货币(美元)相同购买力的标价才是正常的汇率。
比如同样一杯咖啡,日元定价150,美元定价1,汇率就是150:1,如果当前汇率是155:1,那就意味着日元价值被低估,存在升值的预期 — — 因为本来150日元就具备了1美元的购买力。
很多套息交易者会根据这一理论去辅助判断当前某一货币的汇率是否被高估或低估。
由于各国的通货膨胀率是不同的,因此,上述绝对购买力平价理论又进化成相对购买力平价理论 — — 理论上,如果一个国家的通货膨胀率高于另一个国家,那么该国的货币相对于另一个国家的货币也应该贬值,以使得两国商品的购买力平衡。公式如下:

比如同样一杯咖啡,日元定价150,美元定价1,但日本的通胀率是1%,美国的通胀率是3%,通胀率之比1:3,如果日元/美元当前的汇率是150:1,那么未来的汇率应该是147:1(注:相对购买力平价预测了汇率的变化方向和幅度,而非汇率的绝对值)。
因此,如果一国通胀率相对较低,其货币价值被低估,该国的出口商品将变得相对便宜,从而增加了出口需求,带来货币升值预期,回归到购买力平价水平。
以日本为例:日本以其高端制造商品的品质和口碑,获得进口商的青睐,资产价格以外币计价相对被低估,因此日元的价值也处于长期被低估的状态;同时日本国内长期通缩,其货币购买力相对外币也应该升值。因此,如果没有被运输成本和关税等贸易障碍影响的话,日元长期升值预期也更强。
但事实却是,美国在高通胀的情况下,除了增加关税等方式,依靠高利率仍然可以使美元升值,而日元被迫继续贬值。
原因是,尽管货币升值预期和通货膨胀率是套息交易者进行预期回报率计算的基础,但当通货膨胀率差异并不大时(并未出现津巴布韦或委内瑞拉这种恶性通货膨胀),这一因素对汇率的影响也并不明显,而更重要的影响因素是利差。
利率平价理论(Interest Rate Parity, IRP)是货币金融学中的一个基本理论,它解释了不同国家之间的利率差异如何影响货币汇率。一般情况下,在两国利率存在差异的情况下,资金将从低利率国流向高利率国以谋取利润。因此,利率差异会通过汇率的变动进行调整,使得无论投资者选择在哪个国家进行投资,最终的回报率在调整后的汇率基础上应该相等。
2013年,自从安倍经济学实施以后,其政策刺激有利于股市的预期(政府出资购买国债和日股)使得很多外国投资者采取“做多日股+做空日元”的投资组合 — — 即利用低息的日元作为融资货币投资日本国内股市 — — 既规避了汇率风险,又可以获得资产增值的回报。当金融市场动荡、日股下跌时,国外投资者在抛售日股的同时,还需要买回日元为原来的投资组合平仓,造成日元升值。因此,这也造就了美元/日元汇率和日股在走势上的相对一致性 — — 日股下跌,日元兑美元升值。
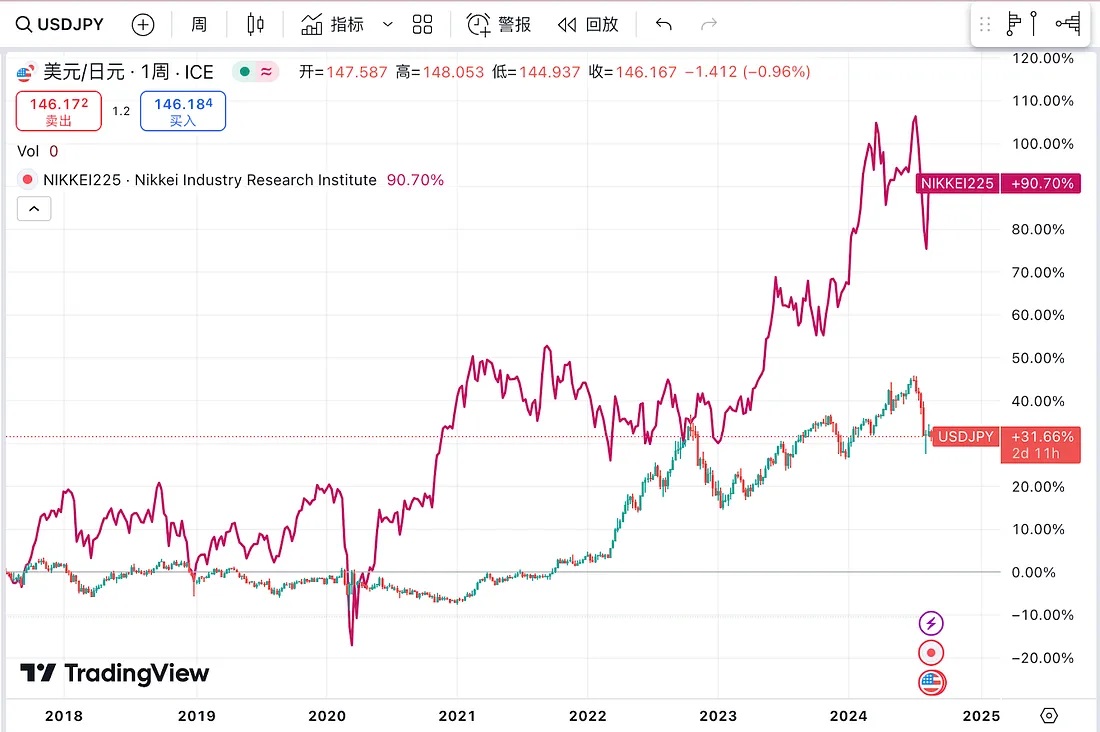
图:日经225走势与美元/日元汇率走势
日元也因此被视为避险货币 — — 一旦出现金融投资市场的波动,套息交易逃离风险就要卖出资产买回日元回补借贷的仓位,日元就会升值。
因此,日元套息交易能够维系和日元的避险属性主要是由日本长期的低通胀(甚至通缩)和特殊的低利率环境支撑的,而政府出资购买国债、股票提供了保障。
3. 货币政策和通胀环境变化威胁日元的稳定
但套息交易的环境近来发生了强烈的变化。
日本2016年开始施行负利率和YCC政策,这一由政府背书、看似稳妥的杠杆套利的诱惑力吸引了更多全球的套息交易投机者。甚至,套息交易者或早已不满足于只投资于日股、美债,更多的高风险资产和大宗商品也被卷入其中。据估算,全球范围内日元的套息交易已不止4万亿美元。
直至2024年3月,日本央行正式宣布结束负利率和退出YCC政策。8年来首次将利率区间从负利率提升到0%到0.1%,7月31日,日本央行出乎意料地再次强势加息到0.25%,日元的套息交易风险再一次被推上风口浪尖。
8月5日,由于日元加息、美元降息预期增强对于日美利差缩小预期所缩造成的套息交易平仓,导致日股的大崩盘甚至美股、韩国、澳大利亚等地区股市均受到影响发生大回撤甚至熔断,让市场对于接下来日本央行的货币政策关注度极大上升。尽管高盛、摩根预测套息交易的杠杆已经清算了一半,日元空头力量也逐渐清零,但不得不警惕,多年来累积的杠杆是否有更深层次的危机潜伏?
而与短期利差变化相比更加重大的变化是,当前日本长期低利率的货币政策和低通胀的环境正在逐步发生变化。
由于俄乌战争带来的国际油价飙升,日本国内通胀已升至2.7%且还在上升趋势,除此之外,日本3月份也已正式宣布退出负利率和YCC政策。近年来日本长期利率水平也在迅速攀升,尽管仍然保持在较低的水平,但显然日本国债的市场将面临更加不确定性的未来。
当前日本央行持有日本国债占比已达50%,更不用提日本250%以上债务/GDP水平已经是全球最高的。随着利率上调,日本政府零利率借贷放水的历史也将远去。
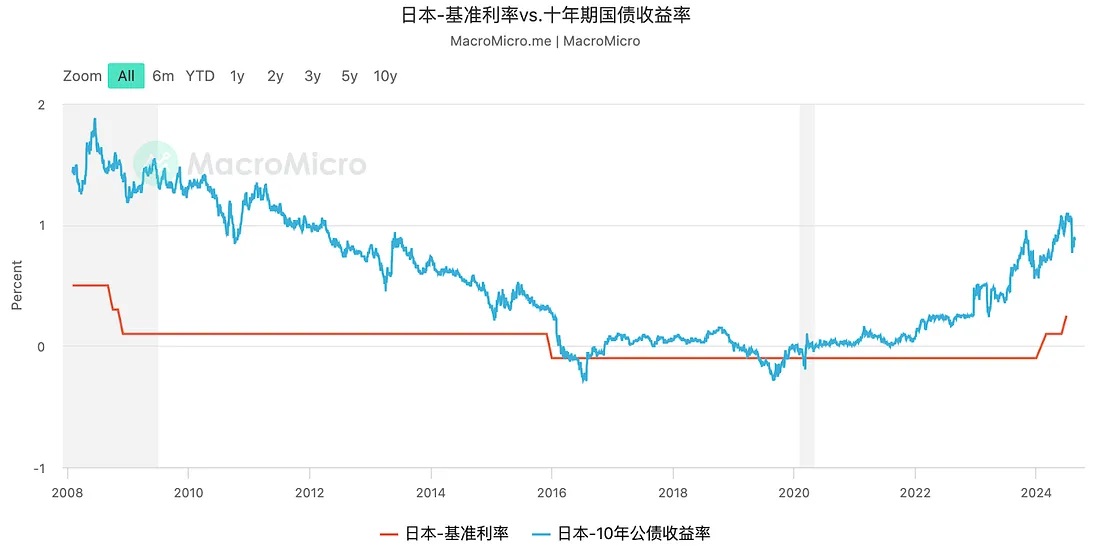
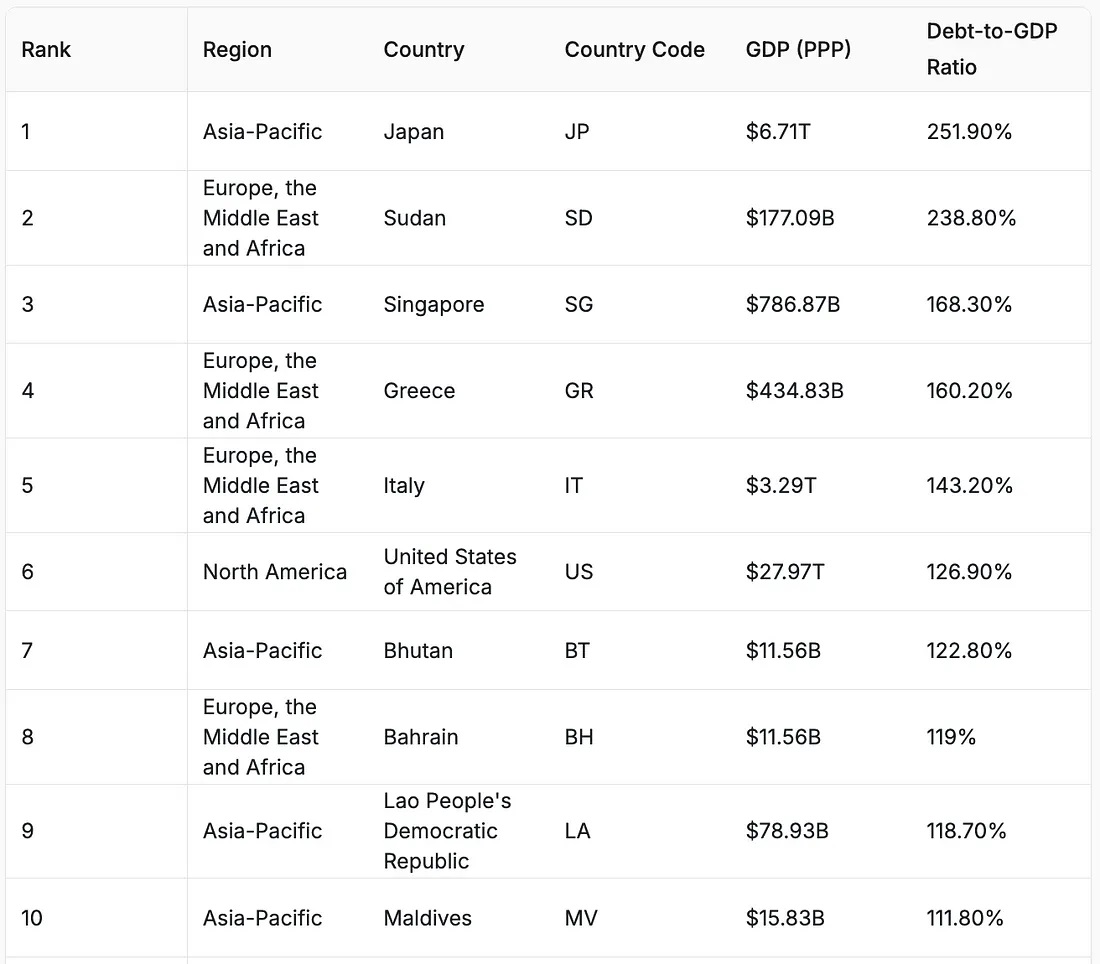
图:全球债务/GDP比例排名,日本居首,美国总量第一
不仅如此,因为日本央行持有巨额国债,如果长期利率上升,就会发生潜在亏损(利息支出与持有国债的收益形成负差价),而如果出售国债就会变成实际亏损。而具体亏损多少取决于国债持有额、偿还期限以及利率上升幅度。
一直以来,日本财政依靠通货紧缩和低利率压缩了利息支出,勉强维持了下来。如果利率恢复到正常水平,仅仅是利息支付就让日本政府难以应对。
如果我们认可日元套息交易能够维系和日元的避险属性是由低通胀和低利率支撑的,那么,随着日本通胀回升、央行退出负利率和YCC政策,再加上日本央行货币政策正常化的渴望、高铸的债台,以及退出宽松货币政策的预期,那么日元的避险属性还能维持下去吗?
4. 最后的救命稻草 — — 外汇干预?
8月5日,套息交易退潮风波导致日股暴跌过后,日本央行高层便紧急发声,称如果金融市场不稳定将暂停加息。随后日元开始迅速升值反弹。市场也在猜测,若美联储开启降息周期,即使日元暂时将不敢继续加息,套息交易退潮未释放的影响力仍有可能再次回归,对维护日本国内金融市场稳定造成威胁。
除此之外,日本利用正常的货币政策进行宏观调控的操作空间再一次受到限制。面对日益上涨的通货膨胀,当前日本央行的处境可谓进退两难。那么,除了利率和央行资产负债表管理工具,还有什么办法能够稳定控制日元的价值呢?答案之一或是通过外汇干预。
根据利率平价理论,理论上,如果一个国家的利率高于另一个国家,高利率国家的货币本身在未来会存在贬值的风险(因为加息的反面是降息的预期),有可能会抵消较高的利率带来的收益。例如近期,随着美元降息预期的增强,欧洲、加拿大等各大央行相继进入降息区间,美元指数已连续下跌至100附近。
鉴于此,投资者一般会利用远期汇率合同来对冲汇率风险。通过签订远期合约,他们可以锁定当前的汇率,以确保在日后能以预定汇率将外币兑换为本币,避免损失。但有时政府会出面干预汇率,让货币在远期市场贬值或升值,使得这一套利机会消失。
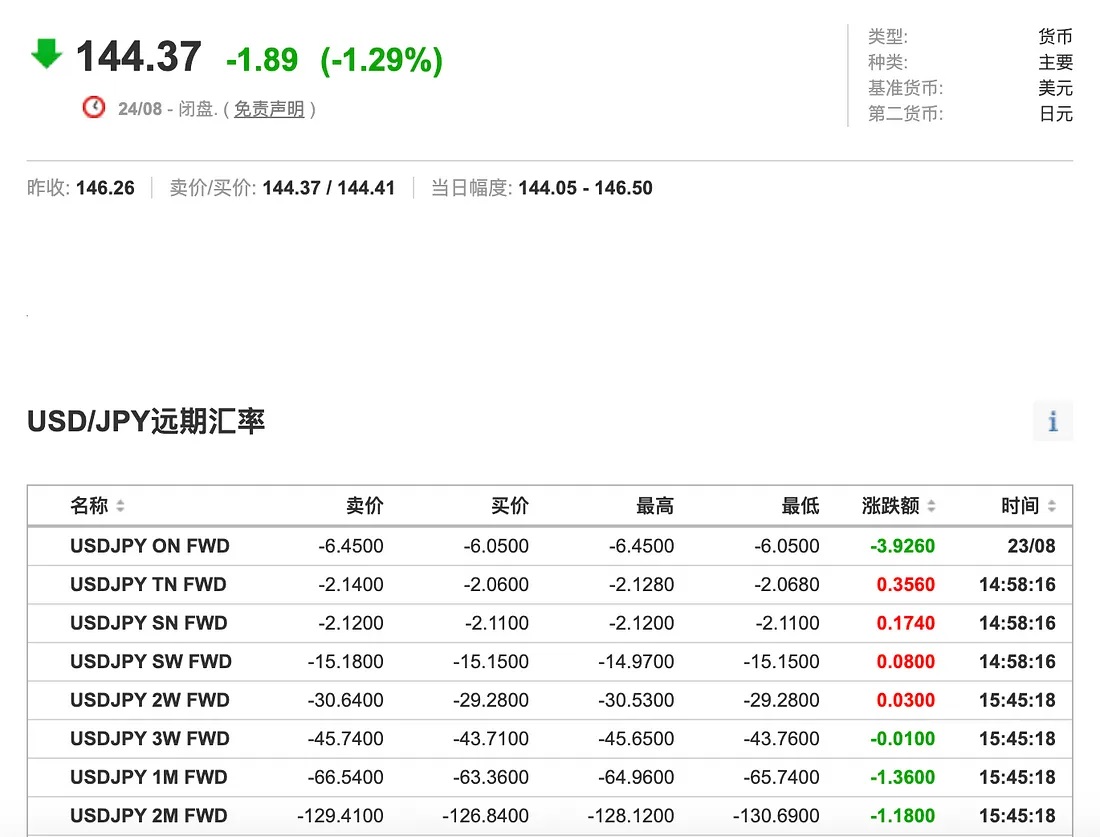
图:2024年8月24日 美元/日元汇率(144.37)与不同期限的远期汇率价格
日本政府进行外汇干预的历史也由来已久。
90年代初,日本经济泡沫破裂后,1995年4月日元对美元汇率升至战后高点79.75日元兑1美元后,日本政府进行了大规模的干预,使得日元汇率在随后几个月内回落到100日元兑1美元以上。
在2003年一年内,日本政府花费了超过20万亿日元(约2000亿美元)进行干预,使日元对美元的汇率保持在110日元兑1美元左右。
随着美联储2022年3月份开始加息以来,日元兑美元的贬值局面一度迫使日本货币当局出手干预。
在2022年9~10月的日元贬值局面下,日本财务省实施了3次买入日元的干预,总计投入9.1万亿日元;短暂的升值之后,时隔一年,日元对美元汇率再次跌破160:1关口后,2024年4月26日至5月29日日本再次进行外汇干预,总额约为9.7万亿日元。
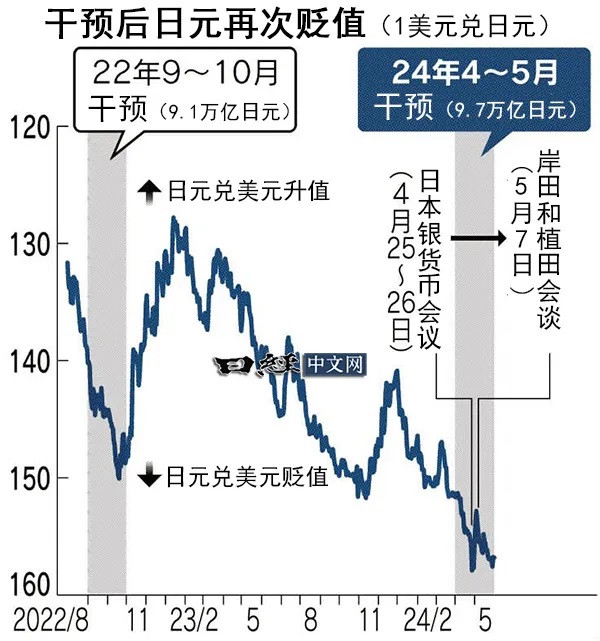
尽管日元升值有助于帮助平衡套息交易、稳定国内金融市场,但是却非常不利于日本出口企业的发展。所以,尽管日元展现出了良好的避险属性,日本财务省(注意,在日本干预汇率决定权属于财务省,日本央行负责实施)也不会任由日元升值。
20世纪90年代以来,日本央行不乏在日元大幅升值时出手干预外汇,尤其是当日元汇率跌至或跌破日本出口商的盈亏平衡汇率时。这一盈亏平衡由日本内阁府调查得出:当日元汇率低于(高于)其水平时,日本出口商将亏损(盈利)。由此可见,日元升值是否损害了其出口,是日本财务省决定是否干预外汇的出发点。
由此可见,日本政府的干预操作通常是在日元急剧升值或贬值的情况下进行,目的是保护日本的经济稳定,特别是维护出口行业的竞争力。
5. 日本维持国际收支平衡的关键 — — 海外投资
而谈到外汇储备和出口,不得不提到一个很重要的概念 — — 国际收支平衡。我们文章一开始就看到了,美国对日本发动贸易战和汇率战的原因就是因为贸易逆差过多。我们经常听到“顺差”和“逆差”,其实指的就是国际收支表的变化。
国际收支平衡表主要部分是经常账户,包括货物和服务贸易以及跨国投资等。其中跨国投资中包括初次收入(Primary Income) — — 跨国投资的收益,如利息、股息、工资等;二次收入(Secondary Income) — — 国际间的转移支付,如赠款、外援、侨汇等。
其它账户还有:资本账户(如移民转移、国际赠予的固定资产等)、金融账户(跨国投资的资本流动,包括直接投资、股票和债券、外汇储备资产等)和储备资产(通常由一个国家的中央银行持有,包括外汇储备、特别提款权SDR、国际货币基金组织中的储备头寸等)。
国际收支平衡对汇率和经济活动的影响十分重要,国际收支账户的变化显示的是一个国家对外经济活动的总体状况。
经常账户顺差表明一个国家在对外经济关系中处于有利地位,而经常账户逆差则意味着可能需要借债来维持对外经济活动。经常账户顺差可能导致本币升值,而逆差则可能导致本币贬值。
这也是各国之所以如此在意出口和汇率的平衡的原因。
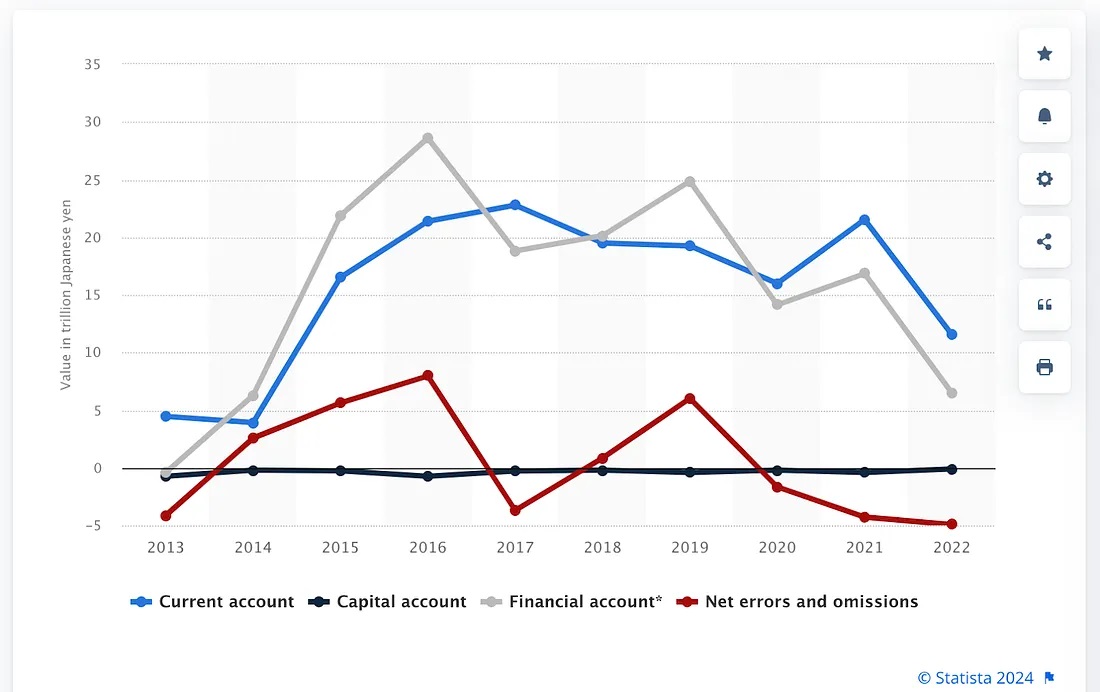
图:日本国际收支账户结构(经常账户current account;capital account资本账户;financial account 金融账户;net errors and omissions差额和遗漏)
注解:Balance of international payments (BoP) in Japan from 2013 to 2022, by category (in trillion Japanese yen) (国际收支平衡表的设计原则是使各账户总和相互平衡,即“总收入”应当等于“总支出”。但是在实际统计过程中,数据往往会存在不完全匹配的情况。这种差额就会被记录在“Net Errors and Omissions”中,以确保表面上账目的平衡)
日本的国际收支平衡表变化主要来自于经常账户,特别是其中的货物贸易和初次收入两个子账户。在全球经济环境或汇率发生变化时,这些账户会对日本的国际收支平衡产生显著影响。
日本是一个出口导向型经济体,制造业尤其强大,出口商品包括汽车、电子产品、机械设备等。因此,货物贸易顺差(即出口大于进口)通常是日本经常账户顺差的重要来源。日本在2013年之前也基本一直保持贸易顺差。
但自2011年福岛核泄漏事件之后,日本需要进口更多的能源,同时2013年后国际油价飙升、日元开始政策性贬值,各种因素叠加使得日本的进口开始大于出口,日本开始频繁产生贸易逆差。
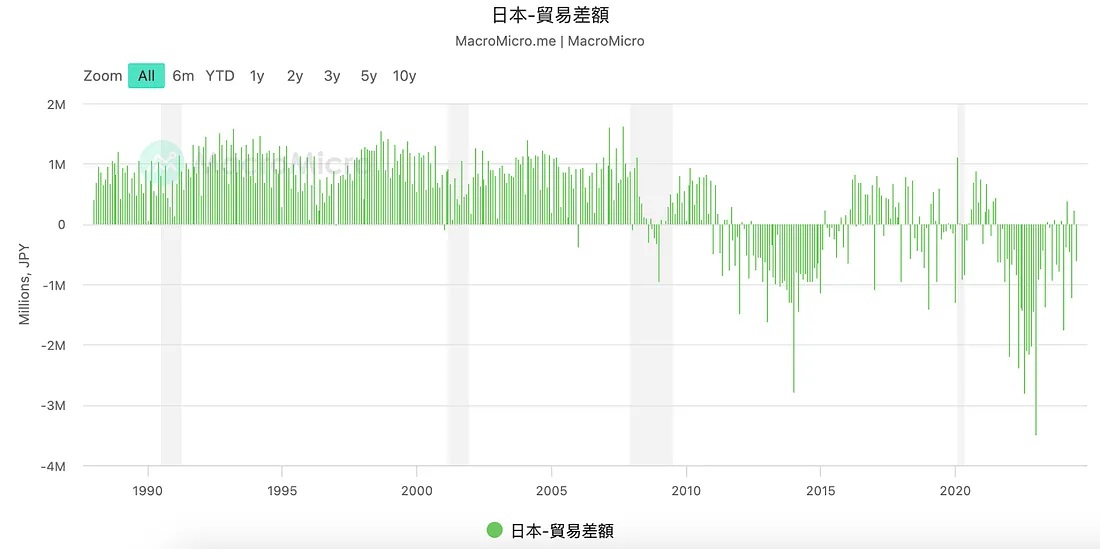
但日本拥有庞大的对外投资组合,尤其是直接投资和证券投资,这使得日本从国外获得大量的利息、股息和其他投资收益。因此,即使在货物贸易顺差减少的情况下,日本仍能通过初次收入账户保持经常账户的顺差。这一部分的收入已经成为近年来日本国际收支平衡表的主要支柱。随着日本国内市场的老龄化和经济增长放缓,海外投资收益的重要性逐渐上升,成为稳定日本国际收支的关键因素。这也是日本能够进行外汇干预的底气。
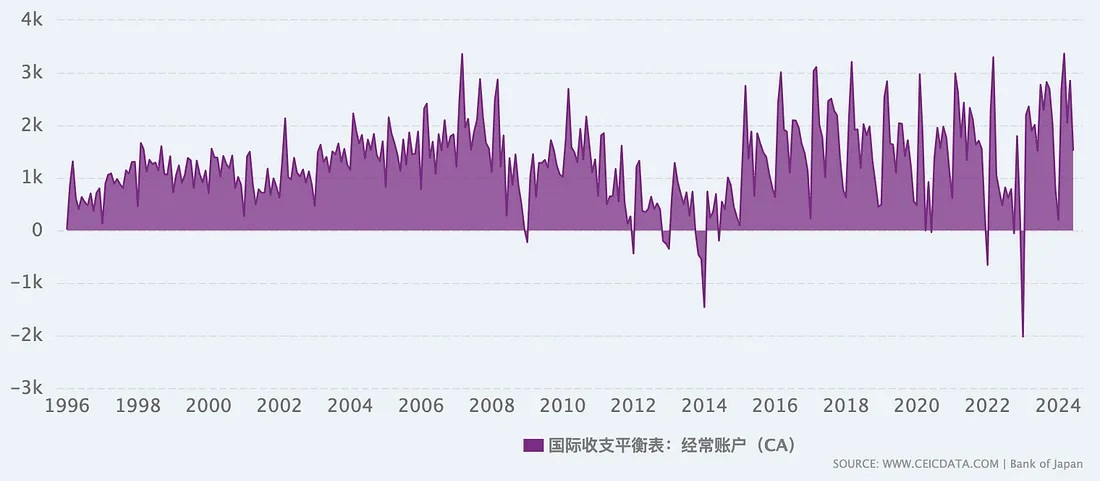
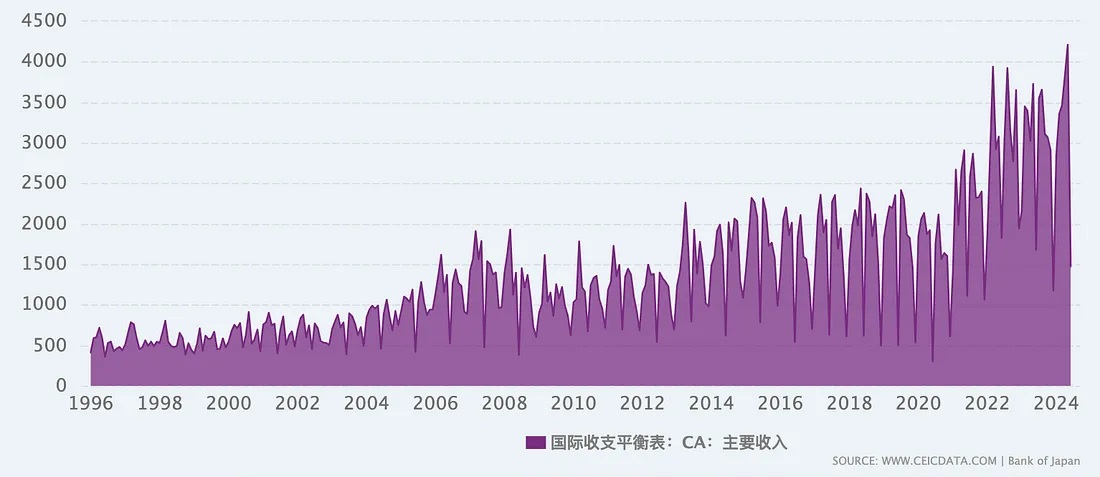
图:日本国际收支平衡表-经常账户-主要收入(prime income)(跨国投资的收益,如利息、股息、工资等)
日本2024年的外汇储备约1.23万亿美元。按照传统的观点,一个国家合理的外汇储备规模应满足六个月的进口需求,或能支付一年内到期的短期外债,或应为一国GDP的9%,以应对因短期资本突然外流而引起的资本账户危机。然而,日本的外汇储备占GDP的比例仅为0.84%(2024年中数据,中国同期外汇储备3.45万亿,占GDP比重21%)。
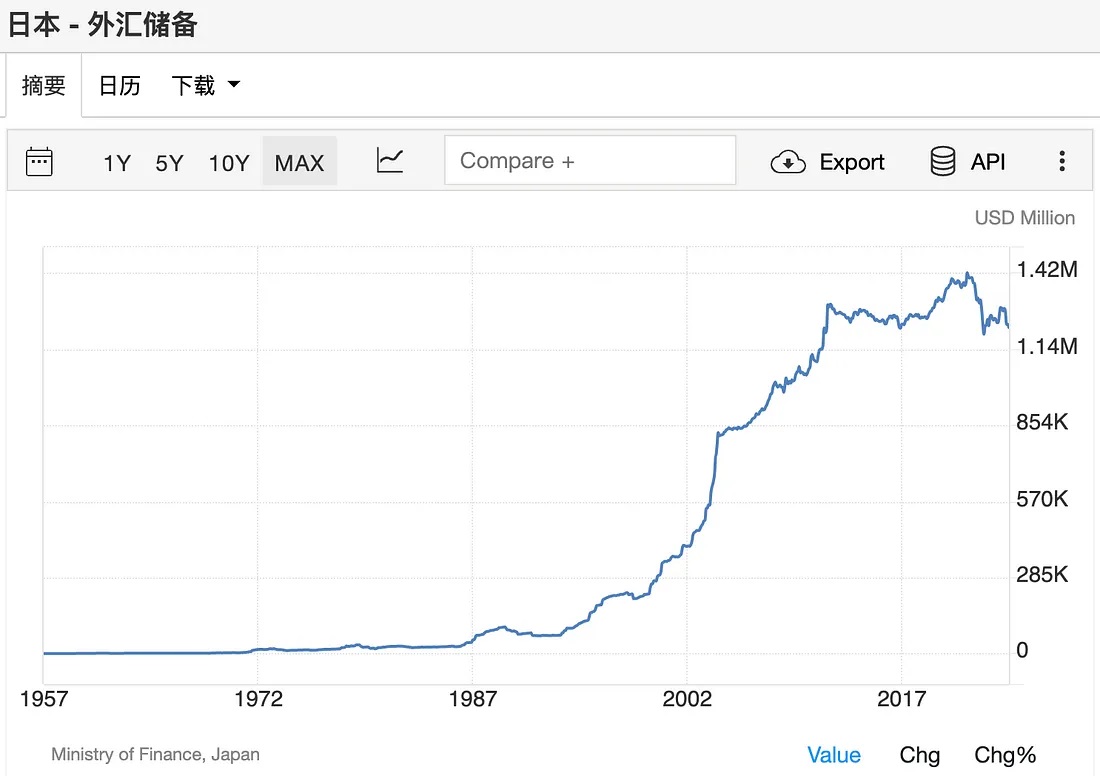
日本近年来如此热衷于购买美债等海外资产,目的也是使其在外汇市场上留有更多回旋的余地。
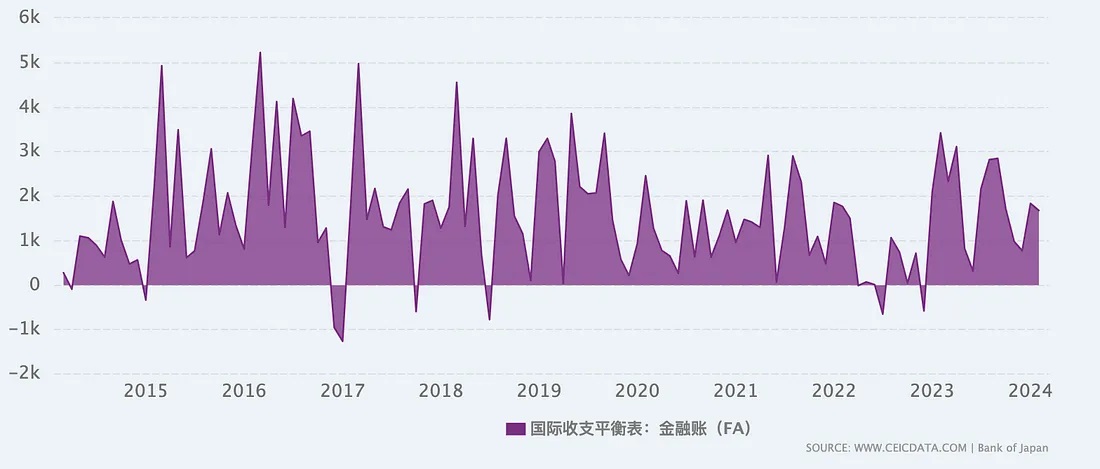
图:日本国际收支平衡表-金融账户(跨国投资的资本流动,包括直接投资、股票和债券、外汇储备资产等,是美债资产所在账户)
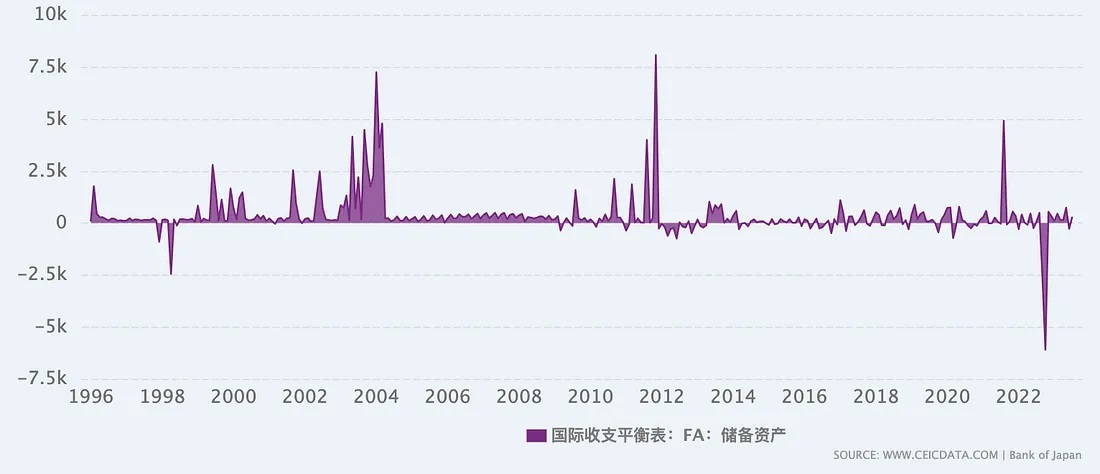
图:日本国际收支平衡表-储备资产(央行持有,包括外汇储备、特别提款权SDR、国际货币基金组织中的储备头寸等)
这些政府干预措施虽然在短期内能够减缓国际金融、贸易冲突带来的影响,但维护本国货币价值的长期效果往往受到全球市场力量和经济基本面的制约。
当全球各国争相以美元/美债(而非贵金属)作为重要储备资产试图缓解货币危机、应对经济和贸易危机时,是否是将自己的命运交予了一个可敌可友的第三人?是否有必要为可能到来的储备资产危机做进一步的打算呢?
至此,我们梳理了广场协议后,由于美国对日本发动贸易战和汇率战,日本政府和央行为了维持国内经济发展和国际贸易,以及日元价值稳定所做的一系列努力。包括通过应对贸易战、国内利率调节、收益率曲线控制、增加对外投资和外汇储备、外汇干预、维持经常账户顺差和平衡国际收支等。我们也了解了在这一过程中由安倍经济学的推广所衍生出的日元特殊的避险属性。最后我们也发现了制定这些宏观调控和政策背后的潜在风险 — — 储备资产之争。
6. 储备资产之争 — — 美债还是黄金?
全球各国的储备资产除了外汇储备、黄金储备、特别提款权SDR还有政府债券、外国国债、国际组织发行的债券等。外汇储备在全球储备资产中占据主导地位,其次是黄金和SDR,而具体的比例因国家和地区的不同而有所差异。
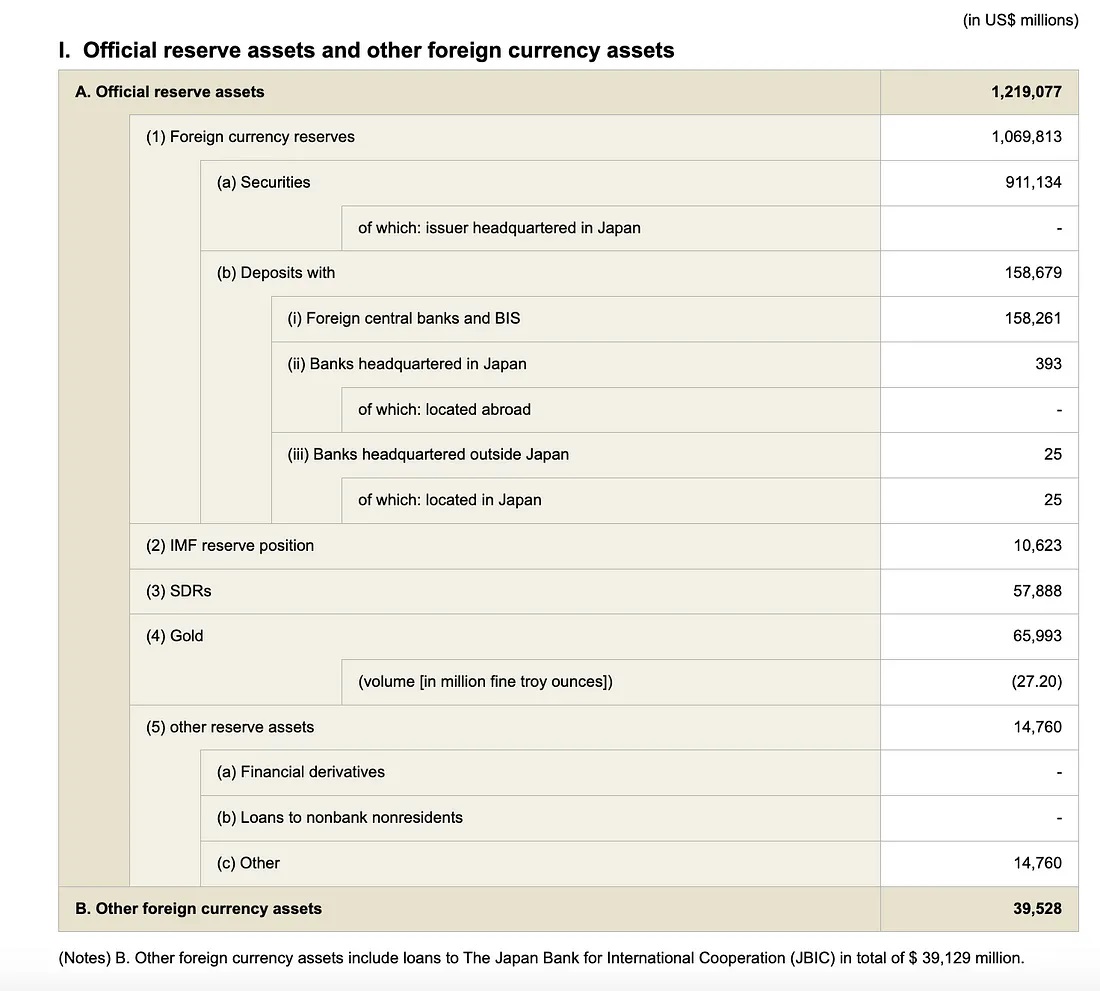
图:日本官方储备资产和外汇资产分类:外汇最多,外汇中以债券为主
近代社会中,主张政府对经济进行干预的历史可以追溯到重商主义,流行于16–18世纪。政府通过关税、补贴、贸易限制等手段来保护和促进本国的产业,国家通过扩大出口、限制进口来实现贸易顺差,积累更多的贵金属(黄金和白银)。
重商主义对欧洲各国的经济政策产生了深远的影响,许多早期资本主义国家(如英国荷兰)通过实施重商主义政策来增强国家实力和财富。
英国在1821年正式采用了金本位制(Gold Standard),成为世界上第一个实行金本位的国家。根据这一制度,英镑的价值直接与黄金挂钩,1英镑对应一定数量的黄金。这一制度为英镑提供了长期的稳定性,使其成为全球主要的储备货币,并巩固了英国作为世界经济强国的地位。
金本位制在英国一直持续到第一次世界大战期间,但在1914年,由于战争支出巨大,英国被迫暂时中止了金本位制。虽然在1925年英国尝试恢复金本位制,但这一制度在1931年全球经济大萧条期间再次被放弃,英镑最终与黄金脱钩。
回顾英镑与黄金脱钩的历史,对英镑的地位产生了深远的影响。在此之前,英镑是全球货币体系的基石,英镑与金本位挂钩,意味着其价值直接与特定数量的黄金相连。这一联系为英镑提供了稳定性和信心,使其成为全球最重要的储备货币。
而英镑与黄金脱钩,控制货币供应和通货膨胀的自动机制消失。没有了黄金的支撑,英镑的价值变得更加容易波动,导致了不稳定性,国际投资者对英镑的信心下降。英镑逐渐失去了世界主要储备货币的地位。随着英镑稳定性的削弱,各国和投资者开始将储备转向仍然与黄金挂钩的美元,这一转变是英国全球经济影响力下降的重要原因之一。
金本位结束后,英国获得了更灵活的货币政策,但也导致了更高的通货膨胀和一系列英镑贬值,进一步削弱了其国际地位。伦敦依然是一个重要的金融中心,但脱离金本位减少了其对全球金融的主导地位。随着美元逐渐成为世界储备货币,美国的影响力上升。
直至1971年,布雷顿森林体系解体后,美元也与黄金脱钩。全球主要货币纷纷转向浮动汇率制度,美元不再维持固定汇率,而是根据外汇市场的供需自由浮动。这使得美元的价值变得更加波动,但也赋予了美国更多的货币政策自主权。
尽管脱离了黄金,美元依然保持其作为全球储备货币的主导地位。由于美元在全球贸易和金融市场中的广泛使用,许多国家继续持有大量美元储备。这巩固了美元作为世界主要储备货币和结算货币的地位。至今,主要国家似乎已经习惯了由美债做锚发行的美元主导全球经济。
而如今逆全球化背景下频发的贸易战与金融战显示,现代社会的国家政府依然受到重商主义的影响,只是干预的手段略有不同,积累的财富形式也从贵金属(黄金)变成了美元和美债 — — 以日本为镜,我们发现在当国家货币、经济、贸易、金融市场被围剿之时,充足的美元/美债储备仿佛是唯一的救命稻草。因此非美国家的经济命脉似乎都与美元/美债的命运深深绑定。
目前,美元仍保持在储备货币中的优势地位,主要原因是:
- 当前国际货币体系中,美元仍是其他货币的锚定物,这就使得美元仍处于国际货币体系的核心;
- 美元在国际贸易结算、跨境融资、国际投资中的广泛使用,具有协同效应和互补性。美元在国际结算中占比在各个货币中排名第一。而美元在所有外贸交易货币中更是占据主导地位;
- 其他货币尚未形成有足够规模、投资级的政府证券市场,支持各国央行储备的投资。而美国国债是国际公认的避险资产,规模也足够大,能为各国央行储备投资提供足够的空间。
但美元/美债也面临着价值贬值的风险:
- 随着美债发行量不断攀升,美国财政税收的利息支出越来越庞大,如果没有新的生产力创造更多税收,一味容忍美国政府借新债还旧债,美债的违约风险加大;
- 美国政府在全球金融市场上的声誉服从于地缘政治的考量,影响美国国债信誉,进而影响到美元的地位;
- 自2008年金融危机以来,美联储和财政部解决经济危机、债务危机的主要方法就是印钞,如果新增货币量大于社会生产力总需求,那么美元的价值必然持续贬值;
- 逆全球化的战略让美国对全球多个主要贸易国发起贸易战、金融战,影响金融资本、商品的自由流通,甚至人才的流通,但是美元得以成为全球主要储备和支付货币的优势就是来自于全球化,逆全球化的趋势并不利于美元的价值稳定。
与黄金的开采呈分布式、且总量有限不同,美元和美债的发行完全由美国政府掌控且没有上限。如果说美债是美国政府用未来的税收收入和国家未来生产能力做背书的借贷,那么毫无节制的借贷和印钞会造成什么样的后果呢?全球是否还会再一次回到金本位制?
政府的宏观调控影响牵一发而动全身,每一次危机发生后都会想尽一切办法让货币价值尽量维持在有利于各方的局面。如果宏观调控被相信具有调节周期的能力,那么为什么市场还是会惧怕加息或降息?是否市场已经不再相信政府每一次都能拯救危机?
我们下一篇继续讨论。

